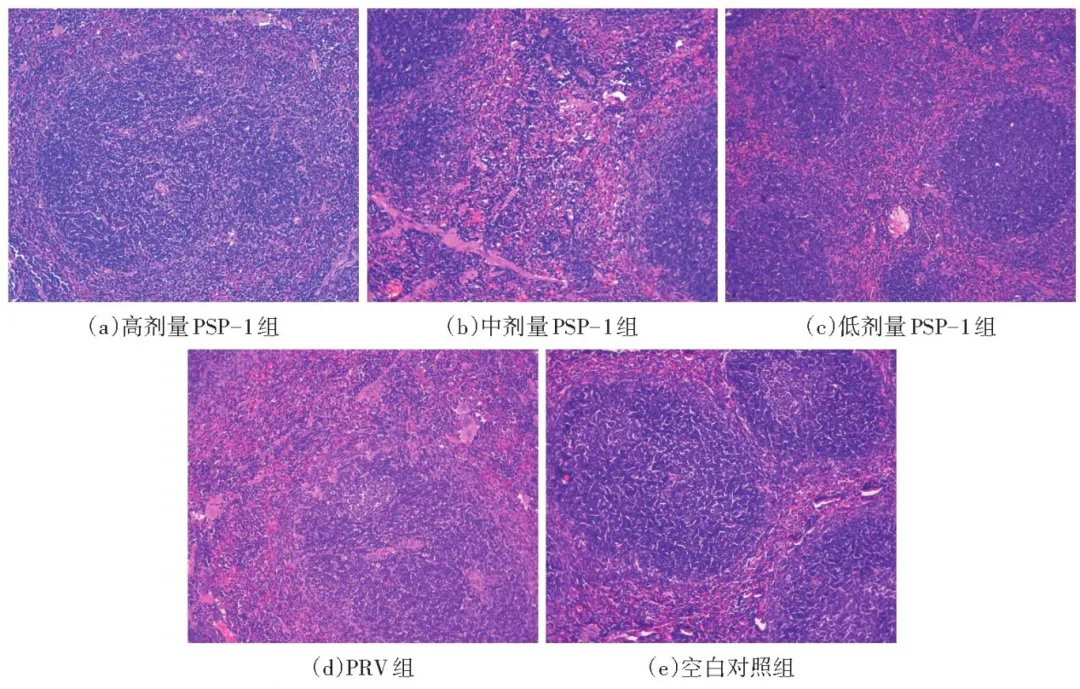
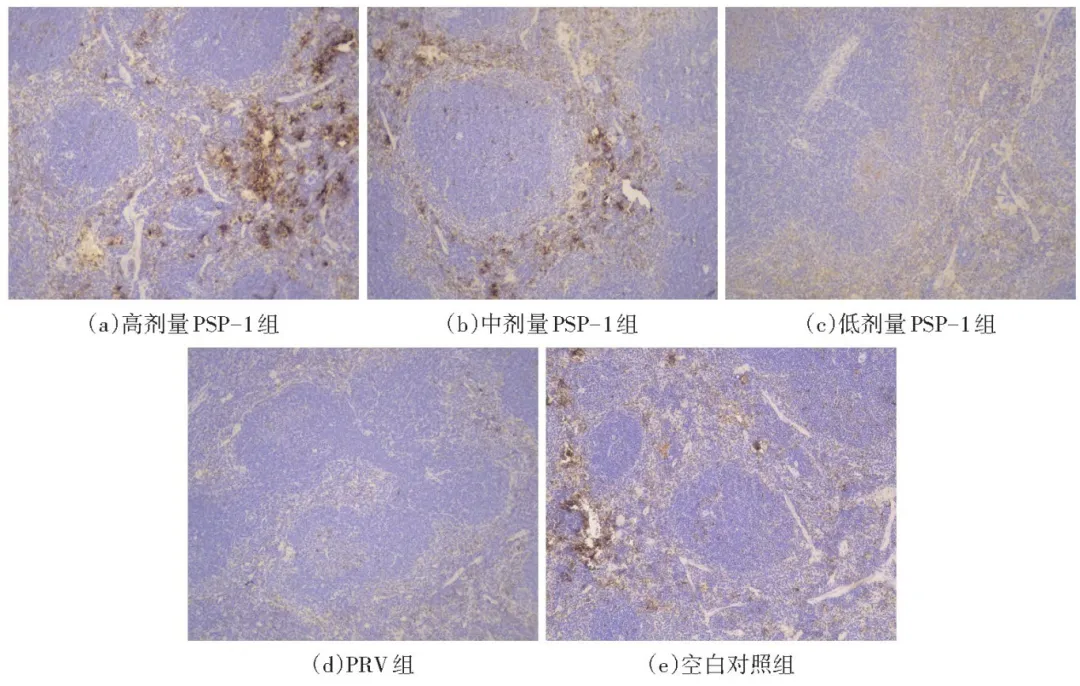
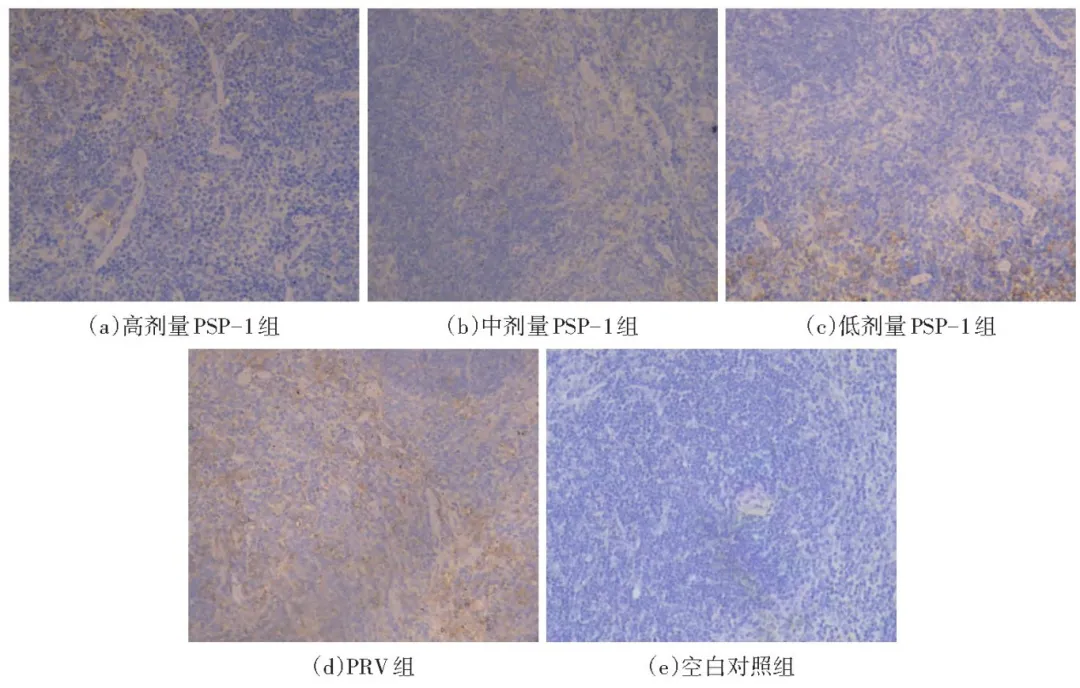
伪狂犬病( pseudorabies,PR )又称Aujeszky病,病原体是伪狂犬病病毒( PRV)。猪是PRV的天然宿主,感染PRV后在不同的生长期表现出不同的症状,母猪主要表现为繁殖障碍,哺乳仔猪主要表现为致死性脑炎和神经系统症状,幼龄仔猪主要表现为呼吸障碍和生长阻滞。PRV主要通过口腔和鼻腔分泌物传播,但也可通过气溶胶和血液传播。在2011年之前中国主要使用疫苗控制猪伪狂犬病的暴发,但自2011年底以来,突变株的出现导致疫苗无法提供针对PRV毒株的完全保护。因此,寻找一种有效的药物预防和治疗PRV具有非常重要的现实意义。 中药中含有许多天然活性成分,多糖就是其中一种,中药多糖具有抗病毒、抗炎、抗氧化等多种药理活性,由于其副作用小的特点在畜禽养殖生产中具有良好的安全性,在PRV的防治中具有广泛的应用前景。螺旋藻是颤藻科螺旋藻属的一种古老低等原核生物,主要分布于热带、亚热带地区淡水及盐碱性湖泊中,富含蛋白质、多糖、多不饱和脂肪酸、维生素等物质 ,螺旋藻含有多种重要组成成分,如多糖、蛋白质、碳水化合物、脂肪酸、维生素、矿物质、叶绿素和β-胡萝卜素。食品和天然药材中的多糖作为一种重要的天然大分子 ,在过去几十年被开发成新的生物活性化合物和候选药物。研究证实,螺旋藻多糖因具有抗癌、免疫调节、降血脂、降血糖、抗血栓、抗病毒、抗氧化、调节肠道微生物等多种促进健康的作用受到广泛关注。目前对螺旋藻多糖的研究主要集中于提取工艺,其抗氧化作用机理仍不明确。本试验选择小鼠作为研究对象,通过建立PRV感染小鼠的体内氧化应激模型,探究PSP-1对PRV感染小鼠脾脏氧化应激的调节作用,为进一步研究螺旋藻多糖在PRV防治中的应用提供依据。 1.1试验材料 1.1.1病毒和螺旋藻多糖组分1(PSP-1) PRV-GXLB-2013株( TCID50=1x107/mL) , 旷大学动物科学技术学院基础兽医学教研室提供。采用酶解水提法制备螺旋藻粗多糖,粗多糖经过DEAE- 52纤维素层析柱和Sephacryl S- 200凝胶层析柱分离纯化,获得纯化多糖PSP-1。PSP-1的多糖含量为94.08%,由9种单糖(葡萄糖、鼠李糖、岩藻糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖醛酸、半乳糖醛酸)组成,主要糖苷键结构方式为:→4)-a-D-Glcp-(1→,糖链连接方式为- +4)-a-D-Glcp-(1→。 1.1.2试验动物 120只无特定疫病( SPF )级的BALB/c小鼠,体重( 20+2) g ,购自长沙市天勤生物技术有限公司,试验动物许可证号: SCXK(湘) 2018-0014。 1.2试验设计 1.2.1分组及处理 将120只SPF级的BALB/c小鼠随机分5组,每组24只,每组4个重复,每个重复6只,分别为高剂量PSP-1(4 mg )组、中剂量PSP-1(2 mg)组、低剂量PSP-1(1 mg)组、PRV组、空白对照组。试验前小鼠禁食12h、禁水6h。高、中、低剂量PSP-1组及PRV组小鼠于第1天腹腔注射PRV病毒稀释液0.2 mL,空白对照组腹腔注射等量生理盐水。随后1~6d高、中、低剂量PSP-1组灌胃不同剂量PSP-1,PRV组和空白对照组灌胃灭菌生理盐水, 0.2 m L/只。第7天将试验小鼠全部处死。取出脾脏,一部分用于超氧化物歧化酶(SOD)、诱导型一氧化氮合酶( i NOS )活性和两二醛( MDA)、一氧化氮(NO)含量测定;另-部分用灭菌生理盐水洗净,吸千水分,采用4%细胞组织固定液固定,于组织病理学观察和免疫组织化学染色。 1.2.2小鼠脾脏氧化应激相关因子的测定 将小鼠解剖,取出脾脏,制备10%的组织匀浆,分别按照组织重( g )和灭菌生理盐水( m L)1 : 9的比例向组织中加入生理盐水,使用组织研磨仪( KZ- II型,购自武汉赛维尔生物科技有限公司)进行研磨制成组织匀浆;再将制备好的组织匀浆3 000 r/min离心10 min,收集上清液,做好标记;严格按照试剂盒的说明进行脾脏组织超氧化物歧化酶( SOD ,批号20200811 )、导型一氧化氮合酶(iNOS ,批号20200811 )活性和丙二醛( MDA ,批号20200813)、一氧化氮( NO ,批号20200812 )含量的测定。所用试剂盒均购于南京建成生物工程研究所有限公司。 1.2.3 H.E.染色观察小鼠脾脏组织学变化 取1.2.1中4%细胞组织固定液固定后的脾脏组织,使用组织石蜡包埋机( YB-6LF型,购自孝感市亚光医用电子技术有限公司)、轮转切片机( RM2245型,购自德国徕卡微系统有限公司)进行石蜡包埋、切片,根据标准流程进行脱蜡和水化。苏木素染色,伊红染艳,脱水封片。在光镜下( 200、400倍)观察各组小鼠脾脏组织学改变情况。 1.2.4免疫组织化学染色检测小鼠脾脏组织中血红素加氧酶1(H0-1)、iNOS的表达 取1.2.3中制备的脾脏组织切片,经过烤片、脱蜡、水化等操作后,使用柠檬酸盐缓冲液浸泡切片以修复抗原。用3%过氧化氢孵育,封闭液( SP试剂盒A液)室温下封闭。根据免疫组化染色试剂盒说明书加入血红素加氧酶1(HO-1 ,批号NBP1-77460 ) /i NOS(批号NBP2-22119 )抗体(抗体均购自NOVUS公司) , 4°C过夜;次日经PBS洗涤后加入二抗( SP试剂盒B液) , 37°C孵育15 min,PBS洗后向载玻片_上的组织滴加三抗( SP试剂盒C液),将温 盒37°C孵育10 ~ 15 min ;再次使用磷酸缓冲盐溶液洗涤,加入DAB显色,苏木素复染,清水冲洗,透明,二甲苯挥发、封片,在显微镜下观察并拍照。黄色或棕色沉积即为阳性表达。 1.3数据处理与分析 试验数据采用Excel表格进行分组统计,采用SPSS 21软件进行单因素方差分析, Duncan' s多重检验进一龀较各组均值,数据均用“平均数t标准差”示。P<0.05为差异有统计学意义。 2.1小鼠脾脏氧化应激相关因子的测定结果 如表1所示,与空白对照组相比,小鼠感染PRV后各组脾脏内MDA、NO含量及i NOS活性显著升高( P<0.05 ) ,而SOD活性显著下降(P<0.05)。与PRV组相比,高、中低剂量PSP- 1组小鼠脾脏中i NOS、MDA含量显著降低( P<0.05) ;高、中剂量PSP-1组脾脏内NO含量活性显著下降(P<0.05) , 高、中低剂量PSP-1组SOD活性显著升高( P<0.05)。 表1 螺旋藻多糖对PRV感染小鼠脾脏氧化应激相关因子的影响(n=24) 注:同列数据肩标不含有相同小写字母表示差异显著( P<0.05) , 含有相同字母表示差异不显著( P>0.05 )。 2.2小鼠脾脏组织病理切片观察 由1可知,白对照组小鼠脾脏在显微镜下未发现病理变化,无明显的淋巴细胞变形坏死现象,红髓白髓结构清晰,界限分明,脾小体结构正常,无明显增大或缩小。PRV组观察到脾小体结构紊乱,白髓界限不清晰,红细胞数量明显增多。剂量、中剂量PSP-1组脾脏结构清晰,几乎不见淋巴细胞变性坏死,红髓和白髓之间界限分明。 2.3小鼠脾脏免疫组化切片观察 2.3.1小鼠脾脏HO-1表达 图2可知,HO-1呈棕色颗粒状, PRV组HO-1表达明显低于空白对照组;与PRV组相比,高、中剂量PSP-1组棕色颗粒明显增多。 2.3.2小鼠脾脏i NOS表达 图1小鼠脾脏组织病理学特征显微图(H.E,400x) 图2小鼠脾脏组织中HO-1表达的免疫组化图(200x) 图3可知,空白对照组未见i NOS表达; PRV组中i NOS表达量最高;与PRV组相比,高、中、低剂量PSP-1组棕色颗粒不同程度减少,其中作用效果最佳的为高剂量PSP-1组。 3.1螺旋藻多糖对PRV感染小鼠脾脏氧化应激相关因子的影响 氧化应激是指机体活性氧( ROS )自由基产生过量与抗氧化防御系统受损的一种氧化还原失衡状态l20。当机体受到有害刺激时产生的活性氧增加,超过机体清除自由基的能力, ROS在体内积累,进而弓|起组织损伤。ROS和由此产生的细胞氧化还原状态变化成为细胞凋亡的诱导因素之一。 研究表明, PRV可在体内外诱发氧化应激(21-23,ROS过量释放,导致细胞氧化和抗氧化系统失衡,从而导致膜脂质的过氧化损伤;同时蛋白质、核酸等物质受到破坏,而导致细胞凋亡、炎症反应、 免疫抑制等。 MDA是脂质过氧化过程分解产生的具有很强生物毒性的次级小分子产物, -方面可以反映体内自由基的活性, 另一方面可以反映出细胞受损程度。 NO、i NOS水平是细胞氧化还原状态的直接指标。SOD是 生物体内一种重要的抗氧化酶吗,将超氧化物歧化为H2O2和O2 ,达到抗氧化应激的作用。Huan研究发现,PRV感染PK15细胞1 h后MDA含量和ROS水平升高。缪卫媛报道,将PRV体外感染猪肺泡巨噬细胞后NO水平在12、24 h时极显著升高,细胞内i NOS活性在8 ~ 24 h时显著或极显著升高, MDA含量在12 ~ 24 h时显著升高。本试验研究结果与上述报道一致,表明PRV感染后小鼠处于氧化应激状态。 图3 小鼠脾脏组织中i NOS表达的免疫组化图(400x) 近年来研究发现,螺旋藻多糖具有一定的抗病毒作用。学者发现 ,螺旋藻多糖通过阻碍病毒颗粒的进入而不是调节干扰素相关细胞因子的表达水平来抑制新加坡石斑鱼虹膜病毒。Chen等发现,螺旋藻提取物可通过在病毒感染早期阶段影响血凝来抑制流感病毒株,提高流感病毒感染小鼠的存活率。王新蕊等[1 9 发现,通过饲喂螺旋藻多糖能提高PRV感染小鼠的抗氧化能力。本试验中,螺旋藻多糖能使PRV感染小鼠脾脏中HO-1表达增多,提高PRV感染小鼠脾脏MDA、NO含量以及SOD活性,与前人研究结果一致,说明螺旋藻多糖能够提高PRV感染小鼠的抗氧化能力。 3.2螺旋藻多糖对PRV感染小鼠脾脏组织学变化的影响 脾脏是机体最大的免疫器官,是机体细胞免疫和体液免疫的中心,同时也是受PRV影响最大的实质器官。感染PRV以后在脾脏会出现中央呈灰白色、外周有红色晕圈的多发性坏死灶。Ren建立PRV感染诱导小鼠炎症模型发现,感染PRV后小鼠脾脏出现红髓增宽、白髓萎缩、脾小体结构紊乱现象。Sun研究发现 , PRV可通过诱导小鼠氧化应激和细胞凋亡相关因子引起脾脏损伤。本试验中, PRV感染后小鼠脾脏出现明显的病理变化,而螺旋藻多糖对PRV感染小鼠脾脏的病理损伤具有一定的缓解作用。 3.3螺旋藻多糖对PRV感染小鼠脾脏组织H0-1、i NOS表达的影响 NOS包括原生型(c NOS )和诱生型(iNOS ) , 细胞在PRV刺激后能产生大量的i NOS和超氧化物阴离子自由基, i NOS可以直接调节NO生成量。HO-1是热休克蛋白家族的成员,是一种重要的抗氧化、抗炎和免疫抑制酶[36],受主要转录因子Nrf2的激活调节。本试验结果表明,螺旋藻多糖能使PRV感染小鼠脾脏中HO-1表达增多, i NOS表达减少,说明螺旋藻多糖对PRV具有 一定的抗氧化作用, PSP-1可能通过提高机体抗氧化能力进而达到抗病毒作用。 小鼠在感染PRV之后使用不同浓度PSP-1 ,能使小鼠脾脏病理变化减轻, NO、MDA含級i NOS活性降低, SOD活性升高。说明PSP- 1对PRV感染小鼠氧化应激反应具有一定程度的调节作用。 原文出处: 仅作科普 侵删 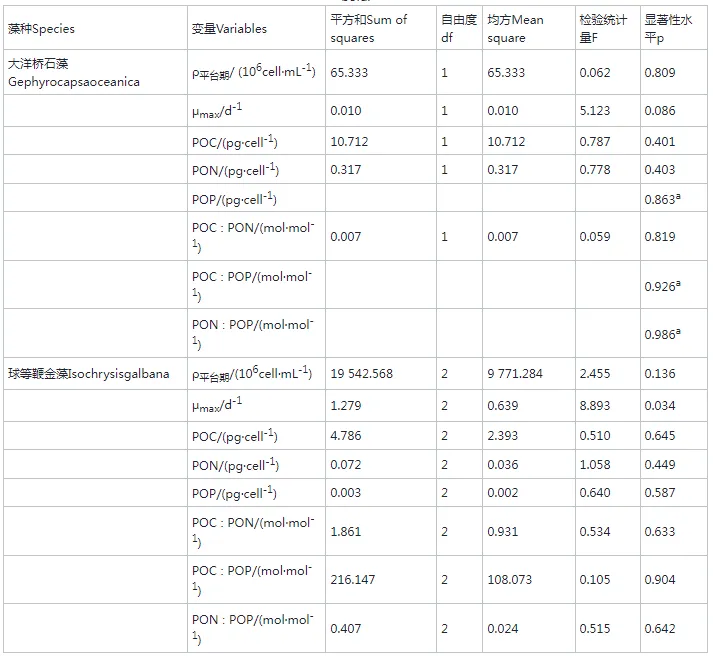
版权归原作者所有