在胃肠道疾病的临床治疗中,口服给药由于具有便捷、安全的优势,往往是首选的给药途径。然而,胃肠道具有复杂的消化环境,许多药物易于被降解失活,某些代谢速度快或水溶性差的药物,则难以突破消化系统的多重生物学屏障,无法达到理想的生物利用度。
为提高口服生物利用度,包括脂质体、胶束、树枝状大分子以及聚合物纳米粒子等在内的多种材料,被设计为口服递送药物的载体。然而,这些递送系统通常面临合成工艺复杂、制造成本高昂、规模化生产条件苛刻等问题,同时易受到生物相容性低、难以降解/代谢以及长期生物毒性等限制,导致临床转化的进程较为缓慢。
因此,开发易于制备生产且安全性良好的口服载体,将对药物口服递送的临床转化具有重要意义。

浙江大学医学院附属第二医院/转化医学研究院周民研究员团队在活性微藻药物递送系统的生物医学应用上取得新进展,在 Science Advances 发表题为 Orally Deliverable Strategy Based on Microalgal Biomass for Intestinal Diseases Treatment 的研究论文。该文被期刊编辑部选为 Cover 封面论文重点推广。

该研究工作开发了一种新的口服给药策略,利用螺旋形天然微藻负载药物姜黄素,将药物输送至肠道组织,用于治疗结肠癌和结肠炎等多种肠道疾病。该口服给药系统利用微藻载体的生物学特性能,提高药物的肠道递送效率和生物利用度,从而发挥更优越的抗肿瘤和抗炎效果。
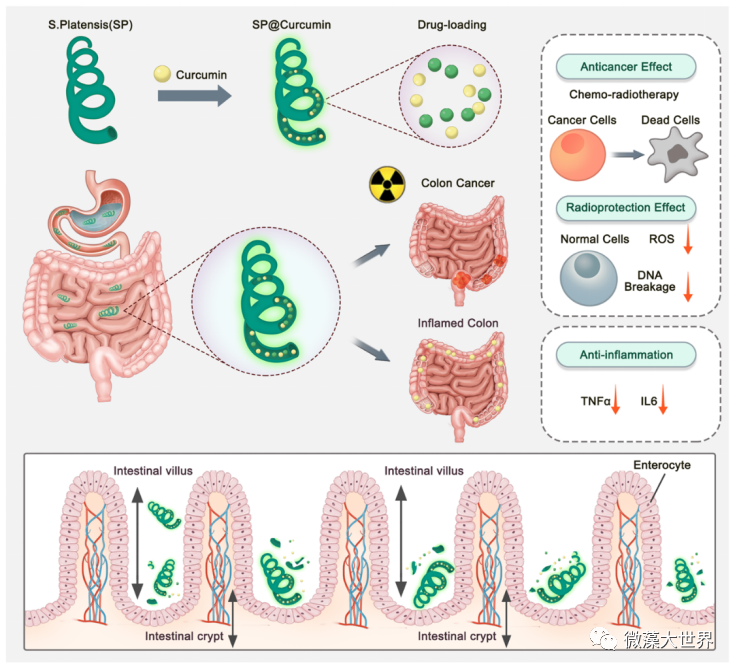
图 1 载姜黄素螺旋藻介导的结肠癌放化疗联合治疗及对肠道炎症的抗炎作用示意图
该螺旋藻载药系统可以在保持结构完整的状态下快速通过胃部,由于其螺旋形的结构特点,相比球形载体,该螺旋状载药系统更易陷入在肠绒毛之间,逐渐降解并释放药物姜黄素,从而延长药物在肠道中的滞留时间及提高药物的吸收效率。
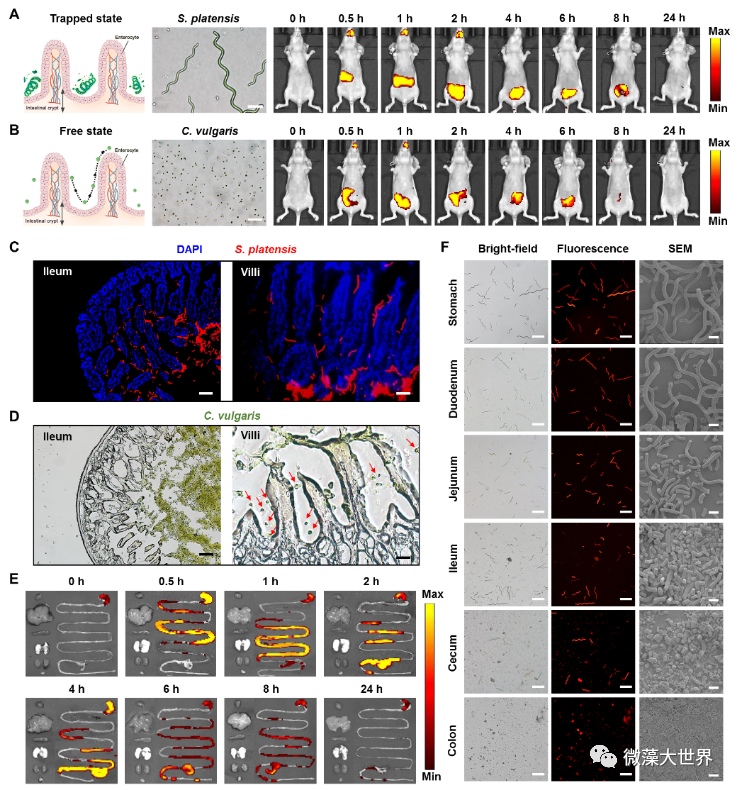
图 2 螺旋藻载药系统的胃肠道分布及生物降解
在原位结肠癌的放射治疗中,该螺旋藻载药系统表现出抑制肿瘤的协同治疗效果。同时,其可作为辐射保护剂,通过消除高剂量 X 射线照射生成的活性氧 ROS、减少 ROS 诱导的细胞 DNA 损伤来保护正常肠道组织。
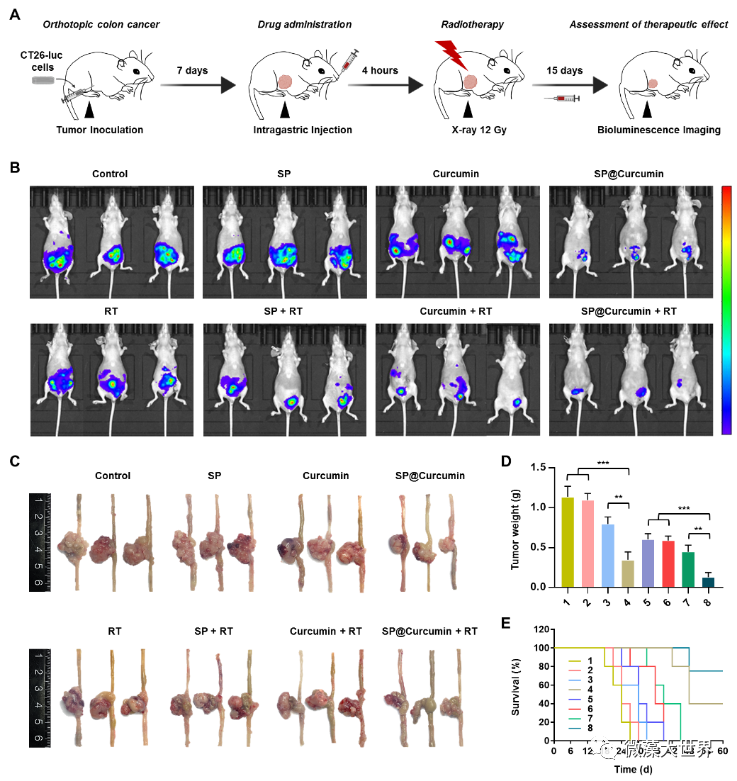
图 3 螺旋藻载药系统介导的放化疗协同治疗抑制结肠癌
另外,本研究还发现了该口服策略在结肠炎治疗中的潜力,其有效降低了 DSS 诱导的结肠炎小鼠的促炎细胞因子水平,有效缓解了结肠炎相关症状和病理表现。
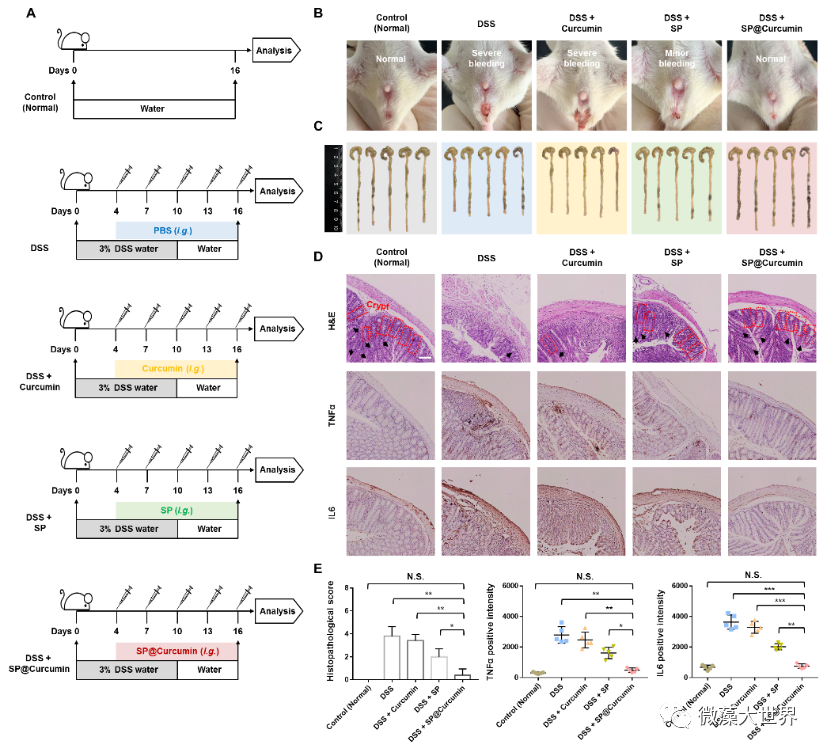
图 4 螺旋藻载药系统对小鼠结肠炎的抗炎作用
作为一种可再生资源,天然活性微藻生产成本低、生物安全性良好,其展现出的良好药物递送性能,更使其成为一种具有潜力的候选药物递送系统。本研究针对肠道疾病所构建的微藻载药系统,不仅为肠癌和肠炎的口服治疗提供了有效的方案,也为药物口服递送系统的设计、开发及临床转化提供了创新性的思路。
浙江大学转化医学研究院周民团队博士生钟丹妮、博士生张东晓和哈佛大学医学院陈纬博士是论文的共同第一作者,浙江大学医学院附属第二医院/转化医学研究院周民研究员和哈佛大学医学院陶伟教授为论文的共同通讯作者。该研究工作得到了浙江大学眼科中心、浙江大学现代光学仪器国家重点实验室等的大力支持,也得到了国家重点研发计划、国家自然科学基金、浙江省重点研发计划等项目资助。
原文链接:
https://www.science.org/doi/10.1126/sciadv.abi9265
来源:丁香学术