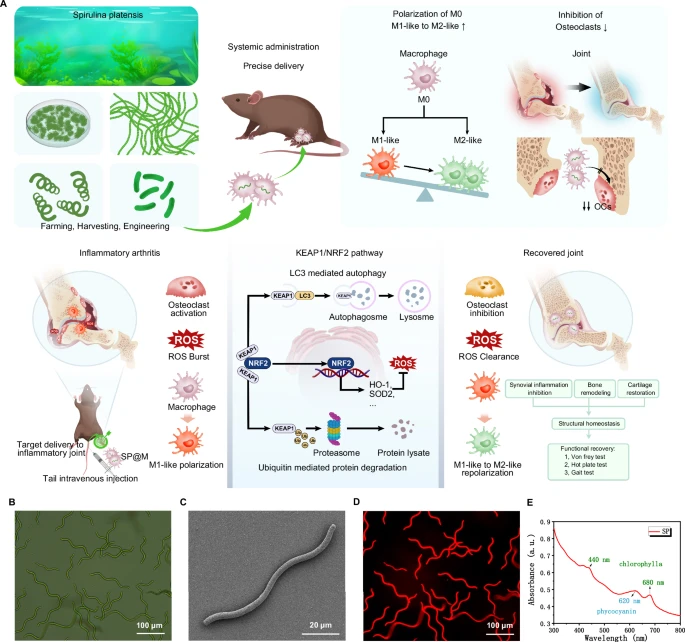
类风湿性关节炎(RA)是一种破坏性的系统性自身免疫性疾病,其特征是严重的滑膜炎和骨质流失,导致关节破坏和畸形。RA的主要病理生理过程涉及免疫系统的异常激活,导致滑膜炎症和随后的骨骼破坏。许多促炎细胞因子和免疫细胞参与这一过程。其中,滑膜巨噬细胞(SMs)是导致病变形成和加重的最突出细胞。SMs分泌各种类型的促炎细胞因子,过量产生活性氧(ROS),然后通过复杂的炎症网络骚扰关节炎滑膜微环境。SMs过度浸润滑膜导致关节免疫功能障碍,加速滑膜炎的进展,并导致破骨细胞活化和最终的骨侵蚀和关节破坏。破骨细胞是从单核-巨噬细胞谱系分化而来的多核巨细胞,负责骨吸收并在骨稳态中起核心作用。在RA的病理环境中,由于滑膜炎症,破骨细胞-成骨细胞轴严重破坏,导致破骨细胞功能增强和RA相关的骨破坏。
如今,症状性RA的临床治疗面临诸多挑战。最常用的治疗方法依赖于几种免疫抑制剂的组合,解决关节炎症。然而,只有三分之二的RA患者达到令人满意的临床缓解。此外,由于免疫系统的抑制,这些免疫抑制治疗通常会增加感染的风险。在RA进展中管理骨重塑也面临同样的困难。通过炎症抑制间接控制骨重塑是模棱两可的。Denosumab(抗核因子-κB配体抗体的受体激活剂)是一种RANKL单克隆抗体,通过与成骨细胞产生的RANKL结合直接抑制破骨细胞药物的骨吸收。它用于另一种破骨细胞相关疾病,即骨质疏松症,但在RA的临床应用中效果有限。这可能归因于不受控制的炎症持续激活炎性破骨细胞的形成。为此,开发新疗法,理想情况下针对关节滑膜炎和炎症相关的骨侵蚀,以及调节那些也可以干扰RA中骨稳态的炎症非依赖性因将有望重塑RA中的骨稳态。
天然钝顶螺旋藻(SP)是全球唯一作为食品进行商业养殖的微生物。它已广泛用于口服肿瘤、肠道疾病和贫血的临床前治疗。最近的研究扩大了SP通过静脉注射在磁驱动和货物输送中的应用,这证明了其作为静脉注射药物的生物相容性和生物安全性。已发现SP含有多种功能化合物,具有潜在的抗氧化、抗炎和免疫调节作用,使其成为处理RA复杂病理学的绝佳候选者。
本研究揭示了SP减轻细胞内氧化应激并促进SMs的促炎M1样至抗炎M2样复极化,重塑氧化还原平衡并抑制滑膜炎症。值得注意的是,SP在直接抑制RANKL诱导的破骨细胞分化方面也很有效,这在重塑RA中的骨稳态中起着协同作用。SP可以靶向巨噬细胞,通过微管相关蛋白1轻链3(LC3)介导的自噬和泛素介导的蛋白酶体降解加速Kelch样ECH相关蛋白1(KEAP1)的蛋白质降解。KEAP1失活后,核因子-e2p45相关因子2(NRF2)的表达和核易位增加,随后促进超氧化物歧化酶2(SOD2)和血红素加氧酶1(HO-1)等抗氧化蛋白的转录,并导致滑膜炎症的缓解。关节炎症的消退可以抑制炎性细胞因子诱导的破骨细胞活化,促进骨侵蚀的缓解。重要的是,SP由巨噬细胞膜(SP@M)设计而成,可在体内实现免疫逃逸和RA靶向。该SP@M恢复了滑膜微环境的平衡,最终在胶原诱导的关节炎(CIA)小鼠模型中实现了骨重塑和软骨修复。与目前RA的治疗方法相比,SP在滑膜炎症和RANKL诱导的破骨细胞分化两个方面的治疗方法更有希望成为缓解RA的现成治疗方法。