糖尿病( DM )作为全球性健康问题, 其患病率逐年上升。DM的主要危害在于导致多个靶器官损害, 并引起多种严重并发症,尤其是心血管疾病。糖尿病心肌病( DCM )作为其引|发的严重微血管并发症之一,已引起国内外学者的高度关注。研究表明, DCM心肌损伤由早期的心肌结构改变,发展为心肌肥大和心肌纤维化,最终导致心功能受损、心力衰竭.因此,阐明DCM心肌损伤发病机制,并探寻DCM的有效治疗药物具有重要意义。铁死亡是一种铁依赖性脂质过氧化导致的新型细胞程序性死亡( PCD )形轼。研究表明,铁死亡在DCM发病机制中发挥着重要作用。当细胞抗氧化系统代谢异常时,铁离子蓄积诱导芬顿( Fenton)反应,导致过多的活性氧( ROS)生;蓄积的ROS与细胞膜上的多不饱和脂肪酸( PUFAs )发生过氧化反应,破坏细胞膜的脂质双分子层,导致细胞膜的解体,发生铁死亡。血红素加氧酶1 ( Hmox1 )作为关键酶在铁死亡上游发挥着重要的调节作用,其通过催化血红素降解而促进细胞内铁蓄积,进而导致铁死亡的发生。因此,者推测,调控Hmox1介导的铁死亡能够改善DCM。
褐藻多糖硫酸酯( FPS )是来源于海藻的天然杂聚糖物质,可用于治疗肝病、心脑血管疾病、肾功能衰竭、动脉粥样硬化等多种疾病。临床研究表明, FPS可明显改善IV型心肾综合征患者心肌损伤指标,保护心功能 ;在动物实验中, FPS可以通过改善氧化应激来减轻DCM心肌损伤。此外,研究表明, FPS能够抑制erastin (铁死亡促进剂)诱导的细胞铁死亡。然而, FPS是否能够通过抑制铁死亡来改善DCM心肌损伤,目前还没有明确答案。更重要的是, FPS是否通过调控Hmox1而抑制铁死亡,其作用机制和分子靶点也不甚清楚。基于此,在本研究中,笔者在体内外探究FPS改善 DCM心肌损伤的作用和机制,以期为FPS治疗DCM心肌损伤提供药理学证据。
1.1动物造模、分组与给药
采用"高脂饲料喂养+ 2次小剂量链脲佐菌素( STZ )腹腔注射”联合措施建立DCM大鼠模型。50只SD大鼠适应性喂养(普通饲料和水) 1周后,采用尾静脉取血法对血糖( BG )及心肌损伤生化指标进行监测后,按照随机数字表法选取8只作为正常组给予普通饲料喂养,余42只大鼠作为造模组给予高脂饲料喂养。造模组大鼠经右侧腹腔注射STZ ( 35 mg-kg-1) , 3 d后重复腹腔注射1次STZ。经大鼠尾静脉采血,每日监测造模组大鼠随机血糖( RBG ),当连续3次RBG均> 16.7 mmol:L-1时,提示DM大鼠模型成功建立。
此后,继续使用高脂饲料喂养造模组大鼠,并检测”血清心肌损伤指标”和“心功能指标”,藉此评价DCM成模标准。 造模结束后,成功建立30只DCM大鼠模型。成模大鼠按照随机数字表法分为3组,每组10只。根据人动物体表面积换算公式计算出大鼠每日的灌胃给药量分别给予正常( normal )组和模型( model )组大鼠生理盐水各1 mL:d- 1灌胃;给予FPS组大鼠FPS混悬液63 mg:kg 1.dT 1灌胃; 给Dapa组大鼠Dapa混悬液0.9 mgkg-1.d-灌胃。共持续6周。
1.2细胞培养与干预
采用高糖( HG )导H9c2细胞建立细胞模型。使用5 mL含10%胎牛血清和1%青霉素链霉素的营养培养基于25T的细胞培养瓶中培养细胞。待细胞密度长至70% ~ 80% ,将其随机分成以下组别:对照( control)组、模型(HG)组、FPS低剂量( FPS-L )组、FPS高剂量( FPS-H )组和Hmox1抑制剂锌原卟啉( zinc protoporphyrin , ZnPP )组。给药时间48 h, HG、FPS-L、 FPS-H、 ZnPP的给药剂量分别为35 mmol:L1、100 μg:mL-1、150 μg:mL-1、10 mmol:L-1.
1.3心肌损伤血清标志物
使佣75 %乙醇消毒大鼠尾静脉,后使佣采血针剌破尾静脉收集血液。针对获取的血样使用贝克曼库尔特AU5421型全自动生化分析仪测定BG及血清心肌酶水平,包括AST、LDH、CK-MB ;采用酶联免疫吸附测定法( ELISA )测定血清BNP水平。以上心肌损伤血清标志物的检测在南京鼓楼医院医学检验中心完成。
1.4心功能指标
各组大鼠使用异氟烷进行麻醉,仰卧固定于操作台,使用Vevo2100型超声影像系统进行彩色多普勒超声心动图检测。采用频率为21 MHz的高频心脏超声探头,待系统准备完成后,进行大鼠左室的M型超声检测,取3个心动周期的平均值记录数据,测量计算大鼠左心室射血分数( ejection fraction , EF )和左心室短轴缩短率( fractional shortening, FS) , 籍此评估大鼠心功能。
1.5心肌组织病理特征
在给药后的第6周末,经腹主动脉采血处死全部大鼠,收集心肌组织标本用于各项指标的检测。将少量心肌组织固定于10%多聚甲醛溶液中,脱水、石蜡包埋,制作成3 μm厚度的病理切片,分别进行苏木精伊红( HE )染色和马松( Masson)染色。在光学显微镜下观察和分析心肌组织的病理特征。
1.6蛋白表达特征
兔疫组织化学( IHC )染色用于检测各组大鼠心肌组织中Hmox1蛋白的表达特征。将上述石蜡病理切片进行常规脱蜡、水化,进行抗原热修复。封闭诟,加入一抗于4 ℃冰箱中孵育过夜。次日,加入二-抗于室温下孵育1 h,并使用二氨基联苯胺(DAB )显色,苏木素复染后,脱水、封片,使用显微镜观察并分析各组大鼠心肌组织中Hmox1的表达特征。蛋白免疫印迹( WB )分析用于检测各组大鼠心肌组织或H9c2细胞中MYH7B、NPPA、 Col- I、a-SMA、 FTH-1、 SLC7A11、 GPX4、4-HNE、Hmox1蛋白的表达特征。 将从-80 °C冰箱中取出的冰冻心肌组织或收集的心肌细胞,经清洗、裂解、研磨匀浆、心、分装、白变性等步骤以提取总蛋白。根据目标蛋白分子量配制分离胶和浓缩胶,然后根据样品浓度上样。通过电泳仪在恒压80 V下分离蛋白,待marker完全分离后加压至120 V。随后将经甲醇激活的聚偏二氟乙烯( PVDF )膜孵至凝胶上,并根据相对分子质量设置湿转程序。使用5%脱脂奶粉封闭PVDF膜1h后,分别用对应的一抗(稀释倍数为1:1 000 )和二抗进行孵育, -抗在4 °C冰箱中孵育过夜,二抗室温下孵育1h。后,用发光液进行曝光显影,并利用ImageJ软件分析条带灰度值,计算蛋白的相对表达量以确定蛋白的表达特征。
1.7心肌组织中亚铁离子( Fe2+ )、ROS和MDA含量
将100 mg冰冻心肌组织样品用磷酸盐缓冲液( PBS )冲洗至无血水后匀浆,离心取上清液,按照Iron Assay Kit说明书检测各组大鼠心肌组织样品中Fe2+含量。将心肌组织切片用ROS染液染色,放置于室温下避光孵育30 min ,染色后使用显微镜观察并分析各组.大鼠心肌组织样品中ROS含量。将10 mg冰冻心肌组织用PBS冲洗至无血水后,加入300 μL Antioxidant PBS溶液匀浆,随后离心取上清液,按照MDA Assay Kit说明书以荧光法检测各组大鼠心肌组织样品中MDA含量。
1.8网络药理学分析
FPS、DCM及铁死亡靶点的收集
根据FPS主要骨架结构 ,通过PubChem数据库获取FPS的SDF分子结构,随后将其SDF结构导入PharmMapper平台,预测FPS的潜在靶点,将靶点通过UniPort数据库平台进行规范化。同时,以"diabetic cardiomyopathy"为关键词, 在OMIM、GeneCards和DisGeNET数据库中挖掘DCM的潜在靶点。此外,通过FerrDb数据库收集铁死亡相关靶点。
FPS治疗DCM的核心靶点的筛选
通过Sangerbox 3.0在线作图平台将FPS潜在靶点、DCM相关靶点与铁死亡相关靶点取交集,得到FPS治疗DCM的铁死亡相关靶点;再将交集靶点提交至STRING 11.0平台获得PPI网络图及拓扑学参数;最后把上述分析结果导入Cytoscape 3.9.0软件,利用其CytoHubba插件,基于degree算法对蛋白互作网络进一步分析得到潜在治疗靶点。
分子对接验证
根据FPS主要骨架结构,通过PubChem数据库获取FPS的3D结构;通过结构生物信息学研究联合实验室( RCSB )蛋白质结构数据库( PDB )获取核心靶点的3D晶体结构。经AutoDockTools 1.5.6软件和PyMOL 2.5软件除去靶点结构中的小分子配体及水分子,并进行加氢、加电荷处理;再运用AutoDock Vina 1.1.2软件进行分子对接操作,从而获得Affinity对接结合能值,并使用PyMOL2.5软件对分子对接结果进行可视化分析。
1.9细胞中Fe2+和ROS含量
采用FerroOrange荧光探针、Highly Sensitive DCFH-DA荧光探针分别检测细胞Fe2+、ROS含量 。将细胞接种于12孔板中,给药干预后移除培养基,用Hank's平衡盐溶液( HBSS )清洗3次,以进行荧光染色。对于FerroOrange荧光染色,每孔加入200 μL的FerroOrange_工作液;对于Highly Sensitive DCFH-DA荧光染色,同样每孔加入200 μL的Highly Sensitive DCFH-DA工作液。在细胞培养箱中避光培养30 min ,染色后,弃去工作液,使用HBSS清洗细胞2次,再加入HBSS于荧光显微镜下观察并检测细胞中Fe2和ROS含量。
1.10电镜观察线粒体形态
将培养好的细胞弃去培养基,不经漂洗,立即加入电镜固定液。收集细胞至离心管中离心( 1 000 rmin-1 , 4 min) , 弃去固定液,加入新的电镜固定液,室温固定2 h ,并使用饿酸于4 °C下固定2 h ,饱和醋酸铀及柠檬酸铅染色,于透射电镜下观察线粒体超微结构变化。
1.11统计学分析
采用GraphPad Prism 8.0软件对实验结果进行统计分析及作图,实验数据以均数+标准差( S )表示。各组数据在接受方差齐性检验后, 采用单因素方差分析( One-way ANOVA )进行统计学处理,当P <0.05或P <0.01时表示差异有统计学意义。
2.1 FPS对DCM大鼠模型BG、心肌损伤及心功能的影响
自造模开始至药物干预后,与normal组相比, model组的BG、BNP和心肌酶( LDH、CK-MB与AST )水平均显著升高( P<0.01) ; 经药物干预6周后,与model组相比, Dapa组的BG明显降低( P<0.01 ) ,而FPS组的BG变化不明显;对于BNP和心肌酶( LDH、CK-MB与AST )水平,与model组相比, FPS组和Dapa组BNP和心肌酶( LDH、 CK-MB与AST )水平均显著降低( P<0.01 )。
此外,经彩超检测分析,与normal组相比, model组的心功能指标EF与FS显著降低( P<0.01 ) ; 给药干预后,与model组相比, FPS组和Dapa组的心功能指标EF.与FS均有不同程度的增加( P<0.01)。结果表明, FPS能改善DCM大鼠模型心肌损伤和心功能(图1 )。
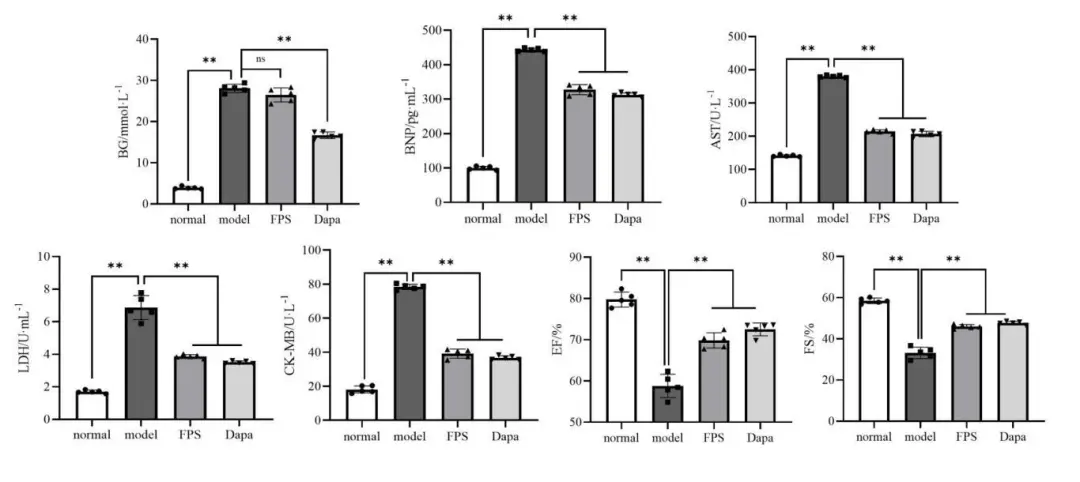
图1 各组大鼠血清生化指标及心功能的比较(x±s, n=5)
2.2 FPS对DCM大鼠模型心肌肥大及心肌纤维化的影响
经光镜观察, normal组心肌细胞排列均匀且整齐,无细胞变形或水肿,心肌纤维完整; model组心肌细胞排列不均、边界较为模糊,细胞出现水肿,心肌纤维间隙增大、排列紊乱;经药物干预6周后,与model组相比, FPS组和Dapa组心肌细胞排列整齐、结构清晰、界限清楚,心肌纤维断裂有所减少。此外,经WB检测分析,与normal组相比, model组心肌组织中心肌肥大标志性蛋白MYH7B和NPPA以及心肌纤维化标志性蛋白Col- I和a-SMA的表达水平明显上调( P<0.01 ) ; 而FPS组和Dapa组,与model组相比,上述4种蛋白表达水平均有所下降( P<0.01或P<0.05 )。结果表明, FPS能改善DCM大鼠模型心肌肥大及心肌纤维化(图2 )。
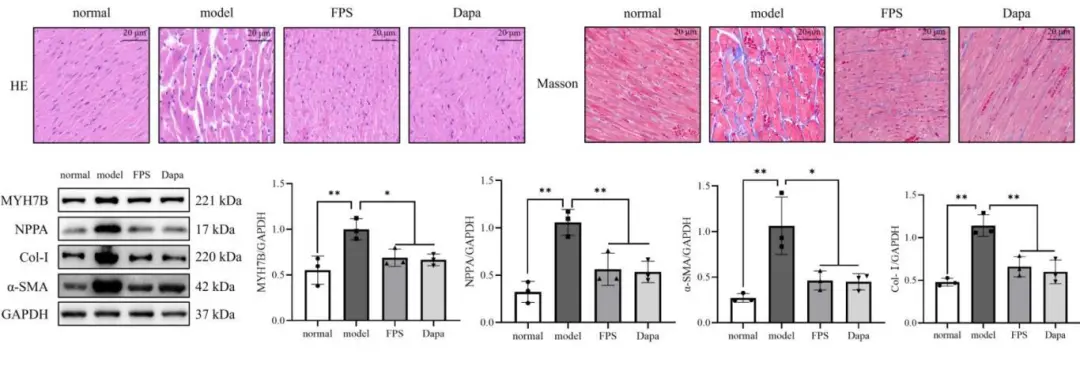
图2 各组大鼠心肌肥大及心肌纤维化的比较( x400;x±s, n=3)
3.3 FPS对DCM大鼠模型心肌组织铁沉积及脂质过氧化的影响
经检测,与normal组相比, model组血清Fe2+、心肌组织Fe2+、心肌组织MDA及心肌组织ROS水平均显著升高(P<0.01) ;经药物干预6周后,与model组相比, FPS组和Dapa组血清Fe2+、心肌组织Fe2+、心肌组织MDA及心肌组织ROS水平显著降低( P<0.01)。结果提示, FPS能减轻DCM大鼠模型心肌组织中铁沉积与脂质过氧化(图3 )。
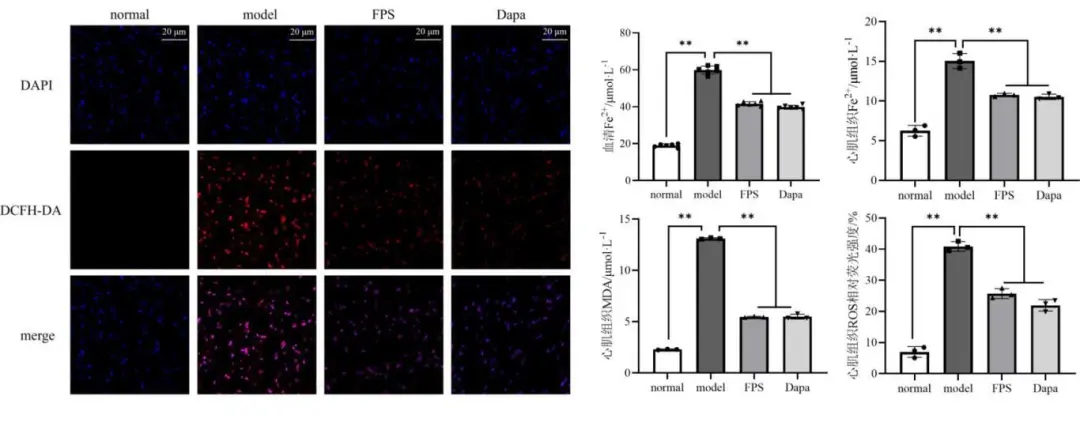
图3 各组大鼠Fe2+. MDA及ROS的比较
3.4 FPS对DCM大鼠模型心肌组织铁死亡相关蛋白表达水平的影响
经WB检测分析,与normal组相比, model组心肌组织中FTH-1、SLC7A11和GPX4蛋白表达水平明显下调, 4-HNE蛋白明显上调(P<0.01 ) ; 经药物干预6周后,与model组相比, FPS组和Dapa组心肌组织中FTH-1、SLC7A11和GPX4蛋白表达水平显著上调, 4-HNE蛋白表达水平显著下调( P<0.01或P<0.05)。结果表明, FPS能不同程度地调节DCM大鼠模型心肌组织铁死亡相关蛋白表达水平(图4)。
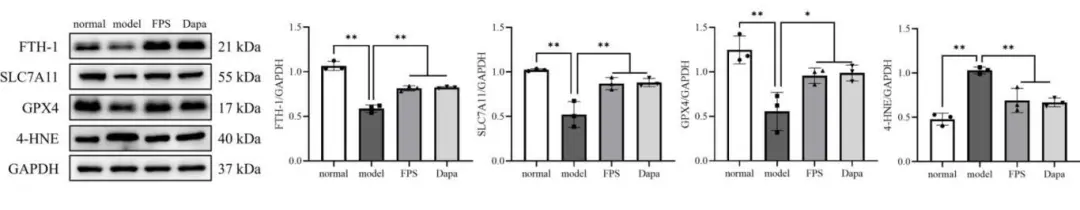
图4 各组大鼠FTH-1、SLC7A11、 GPX4及4-HNE蛋白表达水平的比较(xtS , n=3)
3.5 FPS改善DCM大鼠模型心肌损伤的分子机制探索
经收集筛选得到FPS潜在靶点313个、DCM靶点1 125个、铁死亡相关靶点564个,三者共同靶点14个。"FPS-DCM-FerrDb" 靶点经STRING 11.0平台和Cytoscape 3.9.0软件筛选分析得到排序前10的潜在治疗靶点,其中Hmox1是FPS治疗DCM起关键作用的核心靶点。经AutoDock与PyMOL 2.5软件对FPS和Hmox1进行分子对接和可视化分析,两者结合能ffinity值为-6.2 kcal-mol-1 ,结合活性较好, FPS可以与Hmox1的LEU-141、GLN-145和PHE-169氨基酸残基处形成3个氢键。结果提示, FPS通过调控Hmox1而发挥作用
3.6 FPS对DCM大鼠模型Hmox1蛋白表达水平的影响
经WB和IHC检测和分析,与normal组相比, model组心肌组织中Hmox1蛋白表达水平明显上调( P<0.01 ) ;经药物干预6周后, FPS组和Dapa组心肌细胞中Hmox1蛋白表达水平显著下调( P<0.01)。结果表明, FPS能改善DCM大鼠模型心肌组织Hmox1蛋白的表达水平(图5 )。
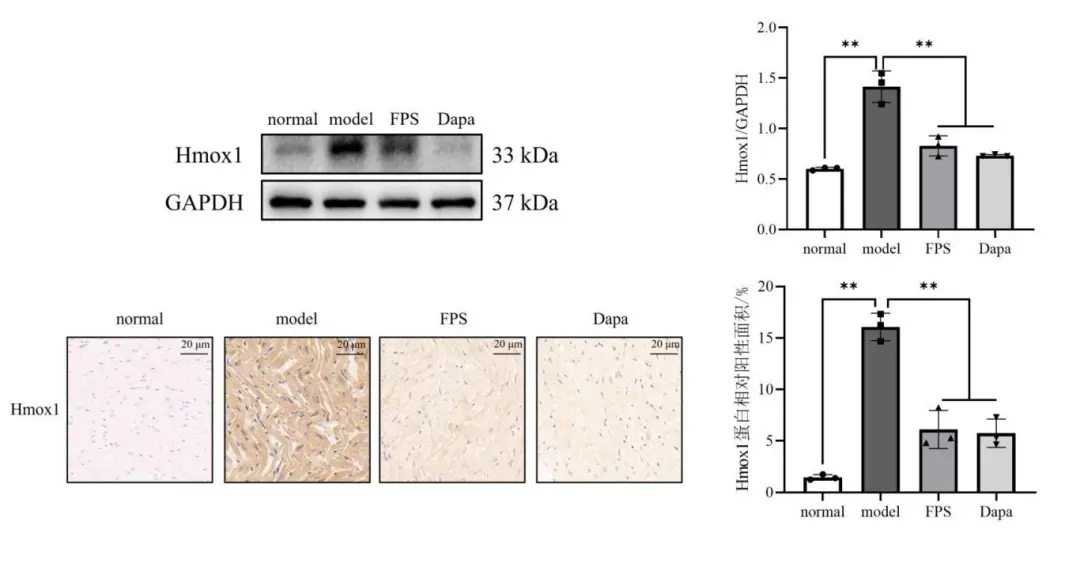
图5 各组大鼠Hmox1蛋白表达水平的比较
3.7 FPS对HG诱导的H9c2细胞铁死亡相关蛋白表达水平的影响
经WB检测分析,与control组相比, HG组细胞Hmox1、4-HNE蛋白表达水平显著上调, FTH-1、SLC7A11、 GPX4蛋白表达水平均下调(P<0.01) ;经药物干预后,与HG组相比,FPS-L组、FPS-H组 与ZnPP组细胞Hmox1、4-HNE蛋白表达水平均下调, FTH-1、SLC7A11、GPX4蛋白表达水平均上调( P<0.01或P<0.05 )。结果表明, FPS能不同程度地调节HG诱导的H9c2细胞铁死亡相关蛋白表达水平,其中FPS-H (高浓度)组的改善程度更佳(图6 )。

图6 各组细胞Hmox1、FTH-1、 SLC7A11、GPX4及4-HNE蛋白表达水平的比较
3.8 FPS对HG诱导的H9c2细胞铁死亡相关指标的影响
经FerroOrange和Highly Sensitive DCFH-DA荧光探针检测,与contro|组相比, HG组细胞的荧光强度明显增强( P<0.01) ;经药物干预后,与HG组相比, FPS-H组和ZnPP组细胞的荧光强度显著减弱( P<0.01) ; 结果表明, FPS能够降低H9c2细胞中Fe2+和ROS水平。此外,经电镜观察, control组细胞线粒体形态正常,边缘清晰,嵴均匀、致密; HG组细胞线粒体出现嵴断裂消失、边界肿胀、模糊等现象;经药物干预后, FPS-H组和ZnPP组细胞线粒体形态有所改善。结果表明, FPS能改善细胞线粒体形态(图7 )。
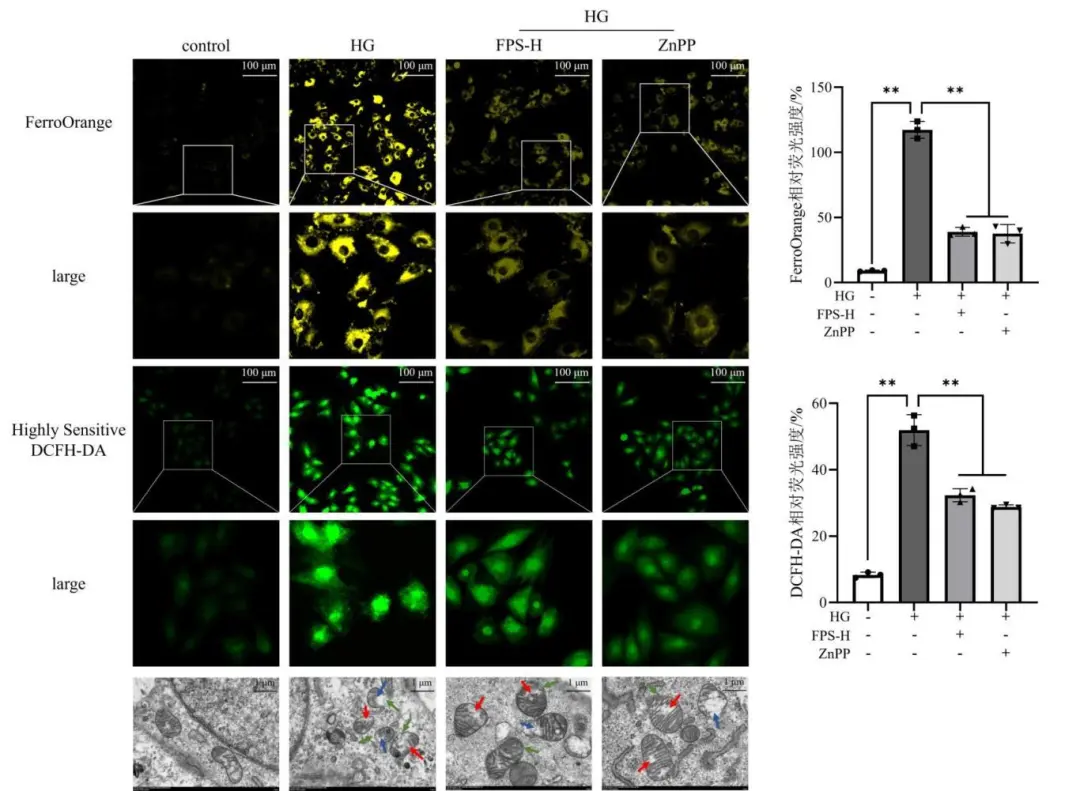
图7 各组细胞Fe2+、ROS及线粒体形态的比较
研究表明, DCM是由DM弓|起的心脏微血管损伤性疾病;在HG环境下,心肌细胞主要能量来源由葡萄糖转向脂肪酸,该过程伴随着耗氧量的异常增高和氧化磷酸化过程的变化,从而引起ROS过量蓄积,导致线粒体结构损伤,进而影响心脏收缩功能。其病变特征主要表现为心肌结构和心功能的异常改变,包括心肌肥大、心肌纤维化、心功能不全等,进而引|起心脏收缩和舒张功能异常,最终,导致心力衰竭的发生。在本研究中,笔者采用“高脂饲料喂养+ 2次小剂量STZ腹腔注射”的方法成功构建DCM大鼠模型,通过检测模型大鼠血清心肌酶水平、心功能、 心肌组织病理特征以及心肌肥大和心肌纤维化标志性蛋白表达水平,笔者发现, DCM模型大鼠LDH、CK-MB、AST和BNP水平显著增高,心功能指标EF和FS降低,心肌组织出现病理性损伤,心肌肥大蛋白( MYH7B、NPPA )和心肌纤维化蛋白(Col-I、a-SMA )表达水平上调。根据这些DCM特征性病变,笔者确认DCM模型大鼠造模成功。
越来越多的研究显示,在DCM的发展过程中心肌细胞铁死亡现象显著,铁死亡诱导的心肌损伤可以作为DCM的潜在治疗靶点。据报道,在DCM的进展中,铁代谢失衡弓|起的铁死亡扮演着关键角色。Hmox1作为细胞内调节血红素代谢的关键酶,通过释放Fe2+.导致铁代谢的失衡,进而促进铁死亡的发生。Hmox1在肿柄菊内酯C诱 导的细胞铁死亡中起关键作用,其使铁离子异常增并促进脂质过氧化;阻断Hmox1信号转导可以改善葡聚糖硫酸钠诱导的铁死亡。在本研究中,笔者发现, FPS能改善DCM模型大鼠心肌组织Fe2+、ROS和脂质过氧化产物MDA水平以及铁储存蛋白FTH-1、抗氧化蛋白SLC7A11和GPX4、脂质过氧化产物蛋白4-HNE的表达水平。简訖, FPS在体内通过抑制铁死亡改善DCM心肌损伤。
在本研究中,基于网络药理学方法,笔者预测FPS作用靶点筛选DCM相关靶点获取铁死亡相关靶点,进而通过分子对接和体内实验分析并验证"FPS-DCM-FerrDb" 关键靶点。结果显示, Hmox1是FPS治疗DCM关键靶点; FPS能够与Hmox1中多个氨基酸残基间形成氢键,两者有较高的对接活性。因此,笔者推测, Hmox1在"铁死亡”诱导的DCM心肌损伤发病机制中发挥着重要作用; Hmox1可能是FPS治疗DCM心肌损伤的靶点。基于此,在体外研究中,笔者采用HG诱导的心肌模型进一步探究FPS治疗DCM心肌损伤的分子机制。结果显示,在HG诱导的H9c2细胞模型中, Hmox1和4-HNE蛋白表达水平明显上调, FTH-1、SLC7A11和GPX4蛋白表达水平明显下调;与Hmox1抑制剂一ZnPP干预组的结果对比 , FPS能明显调节Hmox1和铁死亡相关蛋白表达水平。此外, FPS能降低H9c2细胞内不稳定铁池中Fe2 +含量,提高抗氧化能力,抑制铁死亡,改善线粒体结构损伤。这里,值得注意的是, FPS在体外的上述作用与Hmox1抑制剂ZnPP非常相似。这一结果提示, FPS作为海洋来源的天然药物,很可能是Hmox1的抑制剂。
综上所述, FPS能够改善DCM心肌损伤,其相关机制可能与FPS调控Hmox1进而抑制铁死亡有关;本研究为FPS治疗DCM心肌损伤提供了药理学证据。然而,鉴于FPS的结构复杂性,分子对接分析存在一定的局限性。 未来需以更全面的视角出发,深入探究FPS与Hmox1之间的相互作用,为开发治疗DCM心肌损伤的药物提供坚实的科学依据。
原文出处:
仅作科普 侵删